3.機能性コラーゲンの作製
![]() 3−1.温度応答性コラーゲン材料(図7)
3−1.温度応答性コラーゲン材料(図7)
コラーゲンは動物内で最も多くみられる蛋白質であり、バイオマテリアルとして古くから利用されています。これまでにDDS材料として作製されたコラーゲン材料は、薬物の徐放化材料として使われてきました。本研究では、薬物放出を制御できるコラーゲン材料の作製を目的として、デンドリマーとコラーゲンをハイブリッドさせた材料の作製を行っています。
コラーゲンはグリシン-プロリン-(ヒドロキシ)プロリンの繰り返し配列が多くみられ、三重ヘリックスを形成することによって生体内で機能することが知られています。そこで、その繰り返し配列のペプチドをコラーゲンモデルペプチドとし、薬物運搬体として有用であるデンドリマーの末端に結合させました。すると、ペプチド単独では三重ヘリックスを形成しないのに対して、デンドリマーの末端に集積させることで三重ヘリックス構造を誘起できることがわかりました。そして、この三重ヘリックス構造は熱に応答して可逆的に変化することがわかりました。これは、天然のコラーゲンには見られない性質です。このような熱可逆性を利用したハイロドゲルの作製や温度に応答した薬物の放出制御能についても明らかになってきています。
- Kojima et al, Chem. Lett., 40, 1249 (2011).
- Kojima et al, Soft Matter, 7, 8991 (2011).
- Suehiro et al, Biopolymers, 95, 270 (2011).
- Suehiro et al, Biopolymers, 93, 640 (2010).
- Kojima et al, J. Am. Chem. Soc., 131, 6052 (2009).
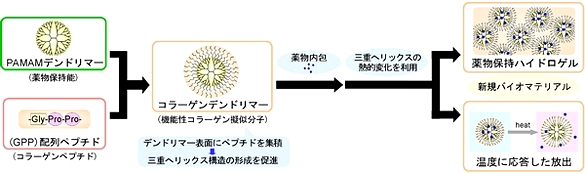
図7 コラーゲンデンドリマーを用いた温度応答性薬物放出
![]() 3−2.癌転移に呼応して作用するDDS材料の作製
3−2.癌転移に呼応して作用するDDS材料の作製
転移は癌に特有の性質であり、癌治療における大きな障壁とされています。癌細胞はコラーゲン分解酵素(MMP)を分泌し、コラーゲンを含む細胞外基質を分解しながら浸潤し、全身へと転移します。我々は、この分子メカニズムを利用した新しいDDS材料の作製を試みています。そこで、MMPによって薬物の放出を制御できる材料として、コラーゲンゲルに薬物運搬体を包埋させたゲルを設計しました。低分子の薬物単体ではなく、薬物運搬体を埋包させることによってゲルからの拡散を抑制し、癌細胞への選択的な送達が期待されます。培養細胞を用いた実験において、薬物運搬体をハイブリッドしたコラーゲンゲルでは転移能の異なる細胞に対して選択的な薬理活性が見られることがわかりました。薬理活性や細胞選択性の向上を目的とした薬物運搬体の改良を行うとともに、in vivoでの性能について検討しています。
このようなゲルは癌の化学療法だけでなく、転移抑制や再発防止にも有用であると考えられます。
- Kojima et al, Acta Biomaterialia, 9, 5673 (2013).
- Watanabe et al, Int. J. Pharm., 446, 81 (2013).
- Kojima et al, Nanomedicine, 9, 767 (2013).
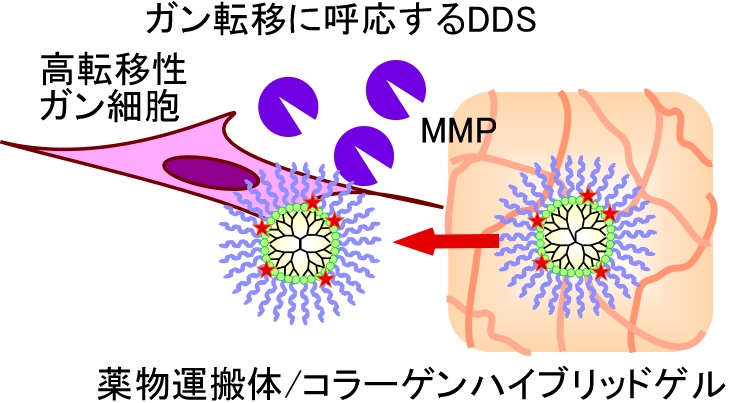
図8 がん転移に応答するDDSの作用機序